|
| O Parkinson afeta cerca de 150.000 pessoas no Reino Unido e mais de 10 milhões de pessoas em todo o mundo. Foto mostra um pesquisador médico (Foto: TOLGA AKMEN / AFP / Getty) |
- Página inicial
- Preliminares
- Mensagem aos Recém Diagnosticados
- Matutando... e alguns textos
- Filmes Recomendados
- Cuidadores
- Habilitar legendas em vídeos Youtube
- DBS - Deep Brain Stimulation
- Celebridades com DP
- Parkinson- Recomeçando a vida (facebook) - artigos produzidos
- Roteiro para pesquisas no blog
- Mal de Parkinson (nosso antigo nome)
Mostrando postagens com marcador terapia genética. Mostrar todas as postagens
Mostrando postagens com marcador terapia genética. Mostrar todas as postagens
segunda-feira, 16 de março de 2020
Esperança de um tratamento eficaz após a descoberta genética
quarta-feira, 4 de março de 2020
Nova técnica de terapia gênica ultrapassa a barreira hematoencefálica, mostra estudo em ratos
MARCH 4, 2020 - Uma nova técnica usando pequenas bolhas e ondas de ultrassom poderia facilitar o caminho para a terapia genética ser entregue ao sistema nervoso central, sugere um estudo em ratos.
A técnica teve um efeito neuroprotetor nos camundongos, e aqueles tratados para modelar o Parkinson mostraram melhorias nas medidas da função motora, segundo o estudo.
O estudo, "Complexo de microbolhas-lipossomas com fator neurotrófico sensível ao ultrassom: investigação pré-clínica para o tratamento da doença de Parkinson", foi publicado no Journal of Controlled Release.
O Parkinson é caracterizado por uma perda de neurônios produtores de dopamina no cérebro. Uma estratégia terapêutica proposta para combater isso é o uso de fatores neurotróficos - moléculas sinalizadoras que promovem o crescimento e a sobrevivência dos neurônios. Exemplos incluem fator neurotrófico derivado de células da glia (GDNF) e fator neurotrófico derivado do cérebro (BDNF), ambos proteínas que são codificadas por genes com o mesmo nome.
Em teoria, esses fatores podem ser administrados terapeuticamente por meio de terapia genética. Em essência, isso envolve a entrega dos genes às células nervosas do cérebro, permitindo que elas produzam mais dessas proteínas e alcancem benefícios terapêuticos.
No entanto, há um problema no uso de terapia gênica que visa células nervosas no cérebro: a barreira hematoencefálica, como o próprio nome sugere, impede que muitas substâncias passem da corrente sanguínea para o sistema nervoso central. Embora isso possa ajudar a proteger o delicado sistema nervoso de danos e infecções, dificulta o direcionamento terapêutico ao cérebro porque é difícil obter compostos terapêuticos (como terapias genéticas) além dessa barreira semipermeável.
Os pesquisadores desenvolveram uma nova técnica de terapia genética para contornar esse obstáculo, contando com o uso de microbolhas menores que um centésimo de milímetro de diâmetro.
Um gene de interesse é inserido em um lipossomo - uma pequena vesícula feita de lipídios (gorduras) - que por sua vez é anexada à microbolha, que é então injetada na corrente sanguínea. O ultra-som direcionado é então aplicado. Quando as ondas sonoras do ultra-som atingem as microbolhas, elas vibram de forma a empurrar fisicamente a barreira hematoencefálica, criando lacunas que facilitam a entrada da terapia genética no cérebro.
Os pesquisadores testaram seu sistema entregando GDNF, BDNF ou ambos, a camundongos - camundongos saudáveis e camundongos tratados com a neurotoxina MPTP, que é comumente usada para modelar a doença de Parkinson.
Essa administração aumentou significativamente os níveis das respectivas proteínas no cérebro dos ratos. O aumento foi observado apenas quando as microbolhas e o ultra-som foram utilizados; nenhum aumento foi observado em experimentos que excluíram esses componentes. Isso sugere que o sistema funcione conforme o esperado.
No modelo de camundongo de Parkinson, o tratamento com terapia genética com GDNF ou BDNF aumentou a produção de dopamina e moléculas relacionadas, enquanto diminuiu a morte celular entre os neurônios produtores de dopamina. Os ratos tratados também mostraram melhorias significativas em várias medições da função motora.
A combinação de GDNF e BDNF não resultou em benefícios acima daqueles conferidos isoladamente. Os pesquisadores sugeriram que isso pode ocorrer porque colocar os dois genes na mesma terapia, como foi feito, poderia limitar a produção de ambas as proteínas individualmente. “Sob a co-expressão do gene GDNF / BDNF, uma conseqüência potencial é que os níveis de expressão do gene GDNF e BDNF falham em atingir níveis terapêuticos”, eles escreveram.
Outras pesquisas podem otimizar esse sistema, permitindo uma exploração mais detalhada de como esses fatores neurotróficos podem ou não interagir sinergicamente.
No geral, o estudo demonstra o potencial de uma nova estratégia de terapia genética para a entrega de terapias no cérebro.
"Nossos resultados indicam que o portador do gene GDNF ou BDNF [foi] associado a uma correção comportamental significativamente maior e à proteção neuronal dopaminérgica", escreveram os pesquisadores, acrescentando que esse sistema forneceu efeitos neuroprotetores para neurônios comprometidos.
"Esses resultados sugerem que o sistema de administração de genes UTMD [baseado em ultra-som e microbolhas] é uma ferramenta valiosa para o desenvolvimento de estratégias terapêuticas para doenças neurodegenerativas", disseram eles. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
quarta-feira, 29 de janeiro de 2020
segunda-feira, 8 de abril de 2019
sexta-feira, 15 de março de 2019
quarta-feira, 13 de março de 2019
Seelos testará o potencial tratamento de Parkinson visando grupos de alfa-sinucleína
MARCH 12, 2019 - A Seelos Therapeutics adquiriu uma licença exclusiva para desenvolver ainda mais uma abordagem de tratamento chamada SLS-007 para a doença de Parkinson, que se destina a diminuir a agregação da proteína alfa-sinucleína.
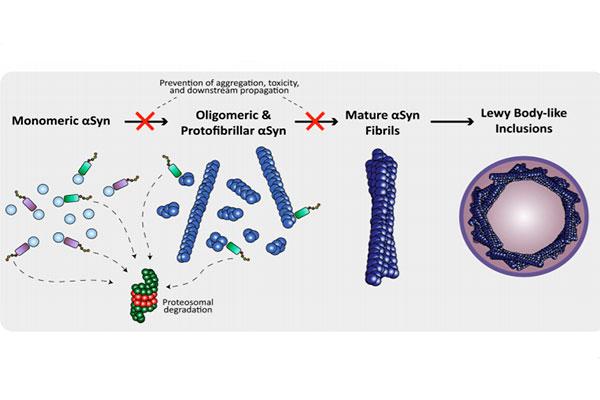
A estratégia terapêutica foi desenvolvida por cientistas da Universidade da Califórnia, em Los Angeles, e inclui uma família de bloqueadores de peptídeos que visam a formação de alfa-sinucleína - um dos principais constituintes dos corpos de Lewy encontrados em pacientes com Parkinson.
O SLS-007 mostrou uma capacidade de retardar a progressão da doença em estudos pré-clínicos, incluindo a capacidade de interromper a propagação e semeadura da alfa-sinucleína - um processo no qual uma “semente” fornece o molde para a agregação de proteína normal em aglomerados preparações e sementes de alfa-sinucleína coletadas de pacientes com demência de Parkinson ou Lewy body.
Ele especificamente tem como alvo uma região central da alfa-sinucleína chamada núcleo do componente não-amiloide, que é particularmente propenso à agregação.
Seelos avaliará se o SLS-007 pode ser administrado em um modelo de camundongo de Parkinson, ao mesmo tempo em que visa estabelecer seu perfil farmacológico in vivo (no corpo) e parâmetros de comprometimento do alvo (a alfa-sinucleína). Além de Parkinson, a empresa planeja testar sua abordagem em outros distúrbios neurológicos.
"A acumulação e agregação de (alfa-sinucleína) é uma característica patológica de (Parkinson)", disse Raj Mehra, PhD, presidente do Seelos, fundador e CEO, em um comunicado de imprensa.
Embora seu papel não seja completamente compreendido, a agregação de alfa-sinucleína parece essencial no desenvolvimento de Parkinson, demência de corpos de Lewy e atrofia de múltiplos sistemas; portanto, "reduzir os níveis de formas patológicas de (alfa-sinucleína) pode alterar o curso de (Parkinson)", disse Mehra.
Tim Whitaker, MD, chefe de pesquisa e desenvolvimento de Seelos, observou a necessidade de desenvolver uma maneira melhorada de restaurar os níveis de dopamina no estriado - uma área cerebral importante para o controle motor - bem como uma terapia segura e eficaz para retardar a doença e progressão do Parkinson, dada a falta de tratamentos modificadores da doença e os efeitos colaterais do uso a longo prazo de tratamentos dopaminérgicos.
"Se formos bem sucedidos em nossos estudos clínicos pré-clínicos e futuros planejados, o SLS-007 pode ser um tratamento desse tipo", disse Whitaker.
A propriedade intelectual desses peptídeos era de propriedade de The Regents, da Universidade da Califórnia. Como parte do acordo, Seelos fez um pagamento inicial de US $ 100.000 para o The UC Regents / UCLA. A empresa também pagará royalties se a terapia chegar ao mercado. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
A estratégia terapêutica foi desenvolvida por cientistas da Universidade da Califórnia, em Los Angeles, e inclui uma família de bloqueadores de peptídeos que visam a formação de alfa-sinucleína - um dos principais constituintes dos corpos de Lewy encontrados em pacientes com Parkinson.
O SLS-007 mostrou uma capacidade de retardar a progressão da doença em estudos pré-clínicos, incluindo a capacidade de interromper a propagação e semeadura da alfa-sinucleína - um processo no qual uma “semente” fornece o molde para a agregação de proteína normal em aglomerados preparações e sementes de alfa-sinucleína coletadas de pacientes com demência de Parkinson ou Lewy body.
Ele especificamente tem como alvo uma região central da alfa-sinucleína chamada núcleo do componente não-amiloide, que é particularmente propenso à agregação.
Seelos avaliará se o SLS-007 pode ser administrado em um modelo de camundongo de Parkinson, ao mesmo tempo em que visa estabelecer seu perfil farmacológico in vivo (no corpo) e parâmetros de comprometimento do alvo (a alfa-sinucleína). Além de Parkinson, a empresa planeja testar sua abordagem em outros distúrbios neurológicos.
"A acumulação e agregação de (alfa-sinucleína) é uma característica patológica de (Parkinson)", disse Raj Mehra, PhD, presidente do Seelos, fundador e CEO, em um comunicado de imprensa.
Embora seu papel não seja completamente compreendido, a agregação de alfa-sinucleína parece essencial no desenvolvimento de Parkinson, demência de corpos de Lewy e atrofia de múltiplos sistemas; portanto, "reduzir os níveis de formas patológicas de (alfa-sinucleína) pode alterar o curso de (Parkinson)", disse Mehra.
Tim Whitaker, MD, chefe de pesquisa e desenvolvimento de Seelos, observou a necessidade de desenvolver uma maneira melhorada de restaurar os níveis de dopamina no estriado - uma área cerebral importante para o controle motor - bem como uma terapia segura e eficaz para retardar a doença e progressão do Parkinson, dada a falta de tratamentos modificadores da doença e os efeitos colaterais do uso a longo prazo de tratamentos dopaminérgicos.
"Se formos bem sucedidos em nossos estudos clínicos pré-clínicos e futuros planejados, o SLS-007 pode ser um tratamento desse tipo", disse Whitaker.
A propriedade intelectual desses peptídeos era de propriedade de The Regents, da Universidade da Califórnia. Como parte do acordo, Seelos fez um pagamento inicial de US $ 100.000 para o The UC Regents / UCLA. A empresa também pagará royalties se a terapia chegar ao mercado. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
sexta-feira, 11 de janeiro de 2019
Terapia gênica poderia eliminar o efeito colateral da droga (L-dopa) em pacientes com Parkinson
11-JAN-2019 - EAST LANSING, Michigan - Um pesquisador da Universidade Estadual de Michigan recebeu uma doação federal de US $ 2,8 milhões para desenvolver uma terapia genética que poderia reduzir e possivelmente eliminar um efeito colateral frustrante de uma droga comumente prescrita para pacientes com Parkinson.
A pesquisa poderia significar um avanço significativo para até 90% dos pacientes que desenvolvem discinesia, um efeito colateral induzido por drogas que resulta no movimento involuntário e descontrolado das mãos, da cabeça e de outras partes do corpo.
O estudo de cinco anos é financiado pelo Instituto Nacional de Distúrbios Neurológicos e Derrames.
A levodopa, um medicamento prescrito para aliviar tremores, rigidez e outros sintomas motores característicos do Parkinson, muitas vezes provoca a condição, e pesquisas anteriores da MSU mostraram resultados promissores relacionados a uma nova terapia gênica.
"Eu tenho estudado maneiras de diminuir a discinesia por anos e nunca vi nada tão efetivo", disse Kathy Steece-Collier, que lidera a pesquisa e é professora do Departamento de Ciências Translacionais e Medicina Molecular no College of Human Medicine.
O estudo se concentrará nas células cerebrais, chamadas de "neurônios espinhosos médios", no corpo estriado, uma área do cérebro associada ao movimento. Esses neurônios têm apêndices, ou dendritos, e cada um deles é coberto por minúsculos espinhos que possuem receptores que interagem com a dopamina, um neuroquímico necessário para a aprendizagem e movimentos motores normais.
Nos pacientes com Parkinson, o nível de dopamina diminui e, como resultado, muitos dos espinhos se retraem, alterando o circuito e causando problemas de movimento.
Steece-Collier disse que, embora a levodopa estimule o crescimento dos espinhos nos neurônios, eles são substitutos ruins para os originalmente perdidos.
"O problema é que os novos espinhos parecem não permitir que os neurônios se conectem normalmente", disse ela. "Com efeito, você começa a enganar, o que pode resultar em discinesia."
Pesquisas preliminares identificaram um canal de cálcio em células cerebrais, conhecido como "CaV1.3", como um potencial alvo terapêutico para aliviar a discinesia. Uma certa quantidade de cálcio é necessária para o funcionamento normal, mas muito pode ser ruim. A perda de dopamina relacionada aos resultados de Parkinson nos canais CaV1.3 é hiperativa, causando muito cálcio e levando à retração dos espinhos.
Algumas drogas estão disponíveis que podem bloquear o CaV1.3, mas é difícil obter uma dose suficientemente grande no cérebro e arrisca efeitos colaterais, incluindo cardiovasculares.
Fredric Manfredsson, professor assistente de ciência translacional e medicina molecular, tem ajudado a Steece-Collier ao desenvolver um vírus inofensivo que, quando injetado no corpo estriado, transporta uma molécula conhecida como "shRNA" para os neurônios e reduz sua capacidade de produzir CaV1. 3
Os resultados iniciais mostraram que esta técnica pode impedir completamente o desenvolvimento de discinesia durante longos períodos de tempo, mesmo quando a dose de levodopa é muito alta. Também pode reverter parcialmente o efeito colateral, algo que antes era difícil de fazer.
"Nunca vimos um efeito tão dramático", disse Tim Collier, professor de neurociência, que também ajudará Steece-Collier a analisar os dados do estudo. "Isso parece quase perfeito em sua capacidade de eliminar esse comportamento."
Segundo os pesquisadores, a nova doação poderia levar a testes clínicos em humanos no futuro próximo e significar uma melhor qualidade de vida para os pacientes com Parkinson. Original em inglês, tradução Google, revisão Hugo. Fonte: Eurekalert.
A pesquisa poderia significar um avanço significativo para até 90% dos pacientes que desenvolvem discinesia, um efeito colateral induzido por drogas que resulta no movimento involuntário e descontrolado das mãos, da cabeça e de outras partes do corpo.
O estudo de cinco anos é financiado pelo Instituto Nacional de Distúrbios Neurológicos e Derrames.
A levodopa, um medicamento prescrito para aliviar tremores, rigidez e outros sintomas motores característicos do Parkinson, muitas vezes provoca a condição, e pesquisas anteriores da MSU mostraram resultados promissores relacionados a uma nova terapia gênica.
"Eu tenho estudado maneiras de diminuir a discinesia por anos e nunca vi nada tão efetivo", disse Kathy Steece-Collier, que lidera a pesquisa e é professora do Departamento de Ciências Translacionais e Medicina Molecular no College of Human Medicine.
O estudo se concentrará nas células cerebrais, chamadas de "neurônios espinhosos médios", no corpo estriado, uma área do cérebro associada ao movimento. Esses neurônios têm apêndices, ou dendritos, e cada um deles é coberto por minúsculos espinhos que possuem receptores que interagem com a dopamina, um neuroquímico necessário para a aprendizagem e movimentos motores normais.
Nos pacientes com Parkinson, o nível de dopamina diminui e, como resultado, muitos dos espinhos se retraem, alterando o circuito e causando problemas de movimento.
Steece-Collier disse que, embora a levodopa estimule o crescimento dos espinhos nos neurônios, eles são substitutos ruins para os originalmente perdidos.
"O problema é que os novos espinhos parecem não permitir que os neurônios se conectem normalmente", disse ela. "Com efeito, você começa a enganar, o que pode resultar em discinesia."
Pesquisas preliminares identificaram um canal de cálcio em células cerebrais, conhecido como "CaV1.3", como um potencial alvo terapêutico para aliviar a discinesia. Uma certa quantidade de cálcio é necessária para o funcionamento normal, mas muito pode ser ruim. A perda de dopamina relacionada aos resultados de Parkinson nos canais CaV1.3 é hiperativa, causando muito cálcio e levando à retração dos espinhos.
Algumas drogas estão disponíveis que podem bloquear o CaV1.3, mas é difícil obter uma dose suficientemente grande no cérebro e arrisca efeitos colaterais, incluindo cardiovasculares.
Fredric Manfredsson, professor assistente de ciência translacional e medicina molecular, tem ajudado a Steece-Collier ao desenvolver um vírus inofensivo que, quando injetado no corpo estriado, transporta uma molécula conhecida como "shRNA" para os neurônios e reduz sua capacidade de produzir CaV1. 3
Os resultados iniciais mostraram que esta técnica pode impedir completamente o desenvolvimento de discinesia durante longos períodos de tempo, mesmo quando a dose de levodopa é muito alta. Também pode reverter parcialmente o efeito colateral, algo que antes era difícil de fazer.
"Nunca vimos um efeito tão dramático", disse Tim Collier, professor de neurociência, que também ajudará Steece-Collier a analisar os dados do estudo. "Isso parece quase perfeito em sua capacidade de eliminar esse comportamento."
Segundo os pesquisadores, a nova doação poderia levar a testes clínicos em humanos no futuro próximo e significar uma melhor qualidade de vida para os pacientes com Parkinson. Original em inglês, tradução Google, revisão Hugo. Fonte: Eurekalert.
sexta-feira, 28 de dezembro de 2018
quinta-feira, 13 de dezembro de 2018
Primeiro Paciente com Dose de Terapia Gênica VY-AADC em Ensaio de Fase 2 de Parkinson
DECEMBER 11, 2018 - First Patient Dosed with VY-AADC Gene Therapy in Parkinson’s Phase 2 Trial.
Veja também aqui: Feb 04, 2019 - Neurocrine, Voyager Team Up to Develop VY-AADC for Parkinson’s Disease e aqui: 22/2/2019 - Voyager Therapeutics stock jumps on 2nd Parkinson's deal.
Veja também aqui: Feb 04, 2019 - Neurocrine, Voyager Team Up to Develop VY-AADC for Parkinson’s Disease e aqui: 22/2/2019 - Voyager Therapeutics stock jumps on 2nd Parkinson's deal.
quarta-feira, 24 de outubro de 2018
Terapia Gênica Mostra Primeiros Sinais da Melhoria do Parkinson
October 23, 2018 - ATLANTA - Uma terapia genética investigativa com adenovírus resultou em melhoria encorajadora nos sintomas da doença de Parkinson para pacientes cuja condição era refratária ao tratamento padrão. A terapia foi bem tolerada e os efeitos foram mantidos por 36 meses, indicam resultados preliminares.
"Até agora, estamos vendo segurança com este tratamento e sinais de um possível benefício clínico", disse o primeiro autor Chadwick W. Christine, MD, PhD, da Universidade da Califórnia, San Francisco, em apresentar os resultados aqui no ANA 2018: 143rd Annual Encontro da Associação Neurológica Americana.
A terapia, chamada VY-AADC01 (Voyager Therapeutics), é injetada diretamente no putâmen. Transfere DNA que codifica a enzima L-aminoácido descarboxilase aromática (AADC), que é considerada chave na conversão de levodopa em dopamina. Os níveis dessa enzima diminuem com o tempo em pacientes com doença de Parkinson.
"Acreditamos que uma razão pela qual o tratamento com levodopa se torna menos eficaz é que, à medida que a doença de Parkinson progride, há uma perda da AADC, a enzima necessária para converter a levodopa em dopamina", disse Christine ao Medscape Medical News.
"VY-AADC01 codifica o gene para AADC", disse ele.
O estudo mais recente da fase 1b da terapia envolveu 15 pacientes com doença de Parkinson que continuaram a experimentar flutuações motoras, apesar do tratamento ideal. Os participantes foram divididos em três grupos, com cinco pacientes em cada grupo.
O grupo 1 recebeu até 450 μl / putamen de VY-AADC01 na concentração de 8,3 × 1011 genomas virais por milímetro (vg / mL). O período de acompanhamento foi de 36 meses.
Grupo 2 recebeu até 900 μl / putamen em 8,3 × 1011 vg / ml, com um seguimento de 18 meses.
Grupo 3 recebeu até 900 μl / putamen em 2,6 × 1012 vg / ml, com um seguimento de 12 meses.
Para garantir a cobertura do putâmen, as infusões bilaterais foram misturadas com o agente de contraste de MRI gadoteridol (Prohance, Bracco Diagnostics).
Os resultados mostraram um aumento na atividade de AADC de uma média de 79% (no grupo 3). Este aumento foi fortemente correlacionado com a cobertura do VY-AADC do putâmen.
Melhorias clínicas, avaliadas com base nas alterações no tratamento dopaminérgico diário de doses equivalentes de levodopa (LED), mostraram reduções médias no LED aos 12 meses de 10,2% no grupo 1; 32,8% no grupo 2; e 39,3% no grupo 3. As reduções foram mantidas aos 18 meses nos grupos 1 e 2.
"Muitos pacientes foram capazes de reduzir a quantidade de levodopa que estavam tomando na dose ou na frequência da dose", disse Christine.
As avaliações dos sintomas também mostraram uma melhora média de 2,3 horas no tempo "on" diário de Parkinson preenchido pelo paciente, representando o tempo com boa mobilidade sem discinesia, aos 24 meses no grupo 1. A melhora foi mantida por 36 meses. No grupo 2, a melhora clinicamente significativa de 3,5 horas no diário de Parkinson "on" foi mantida aos 18 meses.
A melhora correspondente no grupo 3 não foi tão significativa (1,5 horas aos 12 meses); no entanto, os autores observaram que esses pacientes também apresentavam discinesia mais grave no início do estudo.
Melhorias adicionais foram observadas na mudança média nos escores da Escala Unificada de Avaliação de Doença de Parkinson III (UPDRS-III) ON, que reflete as habilidades motoras avaliadas pelo exame médico. As pontuações excederam as definições para "diferenças clinicamente importantes" no grupo 2 (-9,6 pontos) e no grupo 3 (-6,8 pontos) aos 12 meses, com alterações no UPDRS-II OFF (medindo atividades de vida diária) de -3,4 no grupo 2 e -4,4 no grupo 3.
As infusões foram bem toleradas, sem relatos de eventos adversos sérios relacionados ao vetor.
Quatro pacientes apresentaram aumento da discinesia, embora o efeito tenha sido transitório e esperado.
Um paciente apresentou dois eventos adversos graves relacionados à cirurgia (embolia pulmonar e arritmia cardíaca relacionada). Ambos os eventos foram resolvidos completamente.
Christine observou que a embolia pulmonar pode estar relacionada ao longo tempo de infusão cirúrgica.
Em estudos anteriores com infusões menores de VY-AADC e em ensaios clínicos com outros vetores virais, o VY-AADC mostrou pouco benefício. As novas descobertas ressaltam o fato de que o tratamento bem sucedido parece ser dependente do volume, disse Christine.
"Estudos anteriores usando AADC na doença de Parkinson sugeriram que a cobertura no putâmen era inadequada, então os volumes que usamos foram aumentados drasticamente em comparação com os estudos anteriores em torno de 2005 e 2010", disse ele.
Orientação MRI intraoperatória e coinfusão com gadolínio para observar a entrega precisa da terapia gênica também são consideradas fundamentais para o processo. Em tentativas anteriores com terapias gênicas, a entrega inadequada de genes foi um fator limitante.
Com a infusão guiada por MRI com gadolínio, a tomografia por emissão de pósitrons 18F-FDOPA pode detectar a atividade da AADC e fornecer evidências de que a transferência gênica foi bem-sucedida ou não.
"O aumento dependente de dose na captação de gadoteridol é uma medida funcional da atividade da AADC, por isso é uma ótima medida de expressão gênica bem-sucedida", disse Christine.
Os vetores de adenovírus, que atuam como veículos de entrega para terapia gênica, sem colocar em risco o vírus, mostram maior estabilidade e previsibilidade do que outros vetores virais que foram estudados, como os retrovírus.
Conrad C. Weihl, MD, PhD, professor de neurologia da Universidade de Washington em St. Louis, Missouri, disse que a pesquisa oferece insights sobre uma nova direção potencialmente importante para a terapia genética e o tratamento de Parkinson.
"As abordagens de terapia genética são muito novas e inovadoras em geral, e direcionar a entrega para regiões específicas do cérebro, como o putâmen, definitivamente adiciona outra camada de inovação", disse ele ao Medscape Medical News.
Muitas questões permanecem, ele observou.
"Tanto quanto a durabilidade - eu acho que é algo que ainda é desconhecido", disse Weihl.
"A esperança é que eles sejam duráveis e durem por um longo período de tempo - talvez indefinidamente. Quando usamos um tipo específico de vírus, a premissa é que ele é incorporado na célula e persiste na célula, então a única coisa que impede a célula de expressá-la é se a célula morresse", explicou ele.
Weihl observou que as questões de segurança continuarão sendo importantes à medida que a pesquisa avança.
"Preocupações sobre o uso de um vírus estrangeiro incluem um tipo de reação imunológica, e eu acho que essas são coisas que precisam ser feitas com cautela. Então, ir devagar é apropriado porque não queremos causar nenhum dano", disse ele.
O estudo foi financiado pela Voyager Therapeutics. A Dra. Christine e a Dra Weihl não declararam relações financeiras relevantes.
ANA 2018: 143ª Reunião Anual da American Neurological Association. Resumo 80, apresentado em 20 de outubro de 2018. Original em inglês, tradução Google, revisão Hugo. Fonte: Medscape.
"Até agora, estamos vendo segurança com este tratamento e sinais de um possível benefício clínico", disse o primeiro autor Chadwick W. Christine, MD, PhD, da Universidade da Califórnia, San Francisco, em apresentar os resultados aqui no ANA 2018: 143rd Annual Encontro da Associação Neurológica Americana.
A terapia, chamada VY-AADC01 (Voyager Therapeutics), é injetada diretamente no putâmen. Transfere DNA que codifica a enzima L-aminoácido descarboxilase aromática (AADC), que é considerada chave na conversão de levodopa em dopamina. Os níveis dessa enzima diminuem com o tempo em pacientes com doença de Parkinson.
"Acreditamos que uma razão pela qual o tratamento com levodopa se torna menos eficaz é que, à medida que a doença de Parkinson progride, há uma perda da AADC, a enzima necessária para converter a levodopa em dopamina", disse Christine ao Medscape Medical News.
"VY-AADC01 codifica o gene para AADC", disse ele.
O estudo mais recente da fase 1b da terapia envolveu 15 pacientes com doença de Parkinson que continuaram a experimentar flutuações motoras, apesar do tratamento ideal. Os participantes foram divididos em três grupos, com cinco pacientes em cada grupo.
O grupo 1 recebeu até 450 μl / putamen de VY-AADC01 na concentração de 8,3 × 1011 genomas virais por milímetro (vg / mL). O período de acompanhamento foi de 36 meses.
Grupo 2 recebeu até 900 μl / putamen em 8,3 × 1011 vg / ml, com um seguimento de 18 meses.
Grupo 3 recebeu até 900 μl / putamen em 2,6 × 1012 vg / ml, com um seguimento de 12 meses.
Para garantir a cobertura do putâmen, as infusões bilaterais foram misturadas com o agente de contraste de MRI gadoteridol (Prohance, Bracco Diagnostics).
Os resultados mostraram um aumento na atividade de AADC de uma média de 79% (no grupo 3). Este aumento foi fortemente correlacionado com a cobertura do VY-AADC do putâmen.
Melhorias clínicas, avaliadas com base nas alterações no tratamento dopaminérgico diário de doses equivalentes de levodopa (LED), mostraram reduções médias no LED aos 12 meses de 10,2% no grupo 1; 32,8% no grupo 2; e 39,3% no grupo 3. As reduções foram mantidas aos 18 meses nos grupos 1 e 2.
"Muitos pacientes foram capazes de reduzir a quantidade de levodopa que estavam tomando na dose ou na frequência da dose", disse Christine.
As avaliações dos sintomas também mostraram uma melhora média de 2,3 horas no tempo "on" diário de Parkinson preenchido pelo paciente, representando o tempo com boa mobilidade sem discinesia, aos 24 meses no grupo 1. A melhora foi mantida por 36 meses. No grupo 2, a melhora clinicamente significativa de 3,5 horas no diário de Parkinson "on" foi mantida aos 18 meses.
A melhora correspondente no grupo 3 não foi tão significativa (1,5 horas aos 12 meses); no entanto, os autores observaram que esses pacientes também apresentavam discinesia mais grave no início do estudo.
Melhorias adicionais foram observadas na mudança média nos escores da Escala Unificada de Avaliação de Doença de Parkinson III (UPDRS-III) ON, que reflete as habilidades motoras avaliadas pelo exame médico. As pontuações excederam as definições para "diferenças clinicamente importantes" no grupo 2 (-9,6 pontos) e no grupo 3 (-6,8 pontos) aos 12 meses, com alterações no UPDRS-II OFF (medindo atividades de vida diária) de -3,4 no grupo 2 e -4,4 no grupo 3.
As infusões foram bem toleradas, sem relatos de eventos adversos sérios relacionados ao vetor.
Quatro pacientes apresentaram aumento da discinesia, embora o efeito tenha sido transitório e esperado.
Um paciente apresentou dois eventos adversos graves relacionados à cirurgia (embolia pulmonar e arritmia cardíaca relacionada). Ambos os eventos foram resolvidos completamente.
Christine observou que a embolia pulmonar pode estar relacionada ao longo tempo de infusão cirúrgica.
Em estudos anteriores com infusões menores de VY-AADC e em ensaios clínicos com outros vetores virais, o VY-AADC mostrou pouco benefício. As novas descobertas ressaltam o fato de que o tratamento bem sucedido parece ser dependente do volume, disse Christine.
"Estudos anteriores usando AADC na doença de Parkinson sugeriram que a cobertura no putâmen era inadequada, então os volumes que usamos foram aumentados drasticamente em comparação com os estudos anteriores em torno de 2005 e 2010", disse ele.
Orientação MRI intraoperatória e coinfusão com gadolínio para observar a entrega precisa da terapia gênica também são consideradas fundamentais para o processo. Em tentativas anteriores com terapias gênicas, a entrega inadequada de genes foi um fator limitante.
Com a infusão guiada por MRI com gadolínio, a tomografia por emissão de pósitrons 18F-FDOPA pode detectar a atividade da AADC e fornecer evidências de que a transferência gênica foi bem-sucedida ou não.
"O aumento dependente de dose na captação de gadoteridol é uma medida funcional da atividade da AADC, por isso é uma ótima medida de expressão gênica bem-sucedida", disse Christine.
Os vetores de adenovírus, que atuam como veículos de entrega para terapia gênica, sem colocar em risco o vírus, mostram maior estabilidade e previsibilidade do que outros vetores virais que foram estudados, como os retrovírus.
Conrad C. Weihl, MD, PhD, professor de neurologia da Universidade de Washington em St. Louis, Missouri, disse que a pesquisa oferece insights sobre uma nova direção potencialmente importante para a terapia genética e o tratamento de Parkinson.
"As abordagens de terapia genética são muito novas e inovadoras em geral, e direcionar a entrega para regiões específicas do cérebro, como o putâmen, definitivamente adiciona outra camada de inovação", disse ele ao Medscape Medical News.
Muitas questões permanecem, ele observou.
"Tanto quanto a durabilidade - eu acho que é algo que ainda é desconhecido", disse Weihl.
"A esperança é que eles sejam duráveis e durem por um longo período de tempo - talvez indefinidamente. Quando usamos um tipo específico de vírus, a premissa é que ele é incorporado na célula e persiste na célula, então a única coisa que impede a célula de expressá-la é se a célula morresse", explicou ele.
Weihl observou que as questões de segurança continuarão sendo importantes à medida que a pesquisa avança.
"Preocupações sobre o uso de um vírus estrangeiro incluem um tipo de reação imunológica, e eu acho que essas são coisas que precisam ser feitas com cautela. Então, ir devagar é apropriado porque não queremos causar nenhum dano", disse ele.
O estudo foi financiado pela Voyager Therapeutics. A Dra. Christine e a Dra Weihl não declararam relações financeiras relevantes.
ANA 2018: 143ª Reunião Anual da American Neurological Association. Resumo 80, apresentado em 20 de outubro de 2018. Original em inglês, tradução Google, revisão Hugo. Fonte: Medscape.
quarta-feira, 19 de setembro de 2018
Nova abordagem para tratar Parkinson com terapia genética
18 de septiembre de 2018 - Nuevo enfoque para tratar el Parkinson con terapia génica.
sábado, 21 de julho de 2018
quarta-feira, 20 de junho de 2018
sexta-feira, 8 de junho de 2018
sexta-feira, 26 de janeiro de 2018
terça-feira, 28 de novembro de 2017
Nova terapia genética para Parkinson será desenvolvida no Reino Unido
28/11/2017 - Synpromics e UCL colaborarão para desenvolver uma terapia genética para tratar a doença de Parkinson que almeja apenas neurônios específicos envolvidos na doença.
A Synpromics, com sede em Edimburgo, na Escócia, é uma empresa que se concentra no controle de genes. A biotecnológica decidiu colocar sua tecnologia para o desenvolvimento de uma terapia genética para Parkinson em colaboração com o University College London (UCL), uma universidade com uma forte experiência no desenvolvimento de terapias genéticas.
Como parte da colaboração de dois anos, a Synpromics criará promotores de genes sintéticos para controlar a expressão de um gene terapêutico em subpopulações neuronais específicas no sistema nervoso central (SNC). Esta abordagem de abordar apenas alvos específicos tem o potencial de reduzir os efeitos colaterais e tornar a terapia mais segura e eficaz.
Synpromics cria promotores de genes sintéticos projetados para otimizar a expressão em alvos específicos usando seu banco de dados de bioinformática PromPT.
A UCL incorporará os interruptores de genes desenvolvidos pela Synpromics no desenvolvimento de uma terapia genética para doença de Parkinson de início jovem (YOPD) em pacientes que começam a mostrar os sintomas de Parkinson antes de 50.
A terapia de genes para Parkinson não é um conceito novo. No Reino Unido, a Oxford BioMedica já completou um estudo de Fase I / II, onde mostrou que esta tecnologia poderia melhorar a função motora. Nos Estados Unidos, a Voyager Therapeutics completou um teste de Fase I este ano com resultados positivos.
Em comparação, Synpromics e UCL ainda estão em estágio inicial, mas sua abordagem para tornar o tratamento altamente específico pode trazer uma diferença em termos de segurança e eficácia. Especialmente em uma doença em que novos tratamentos são necessários desesperadamente. Este ano, a primeira droga nova para Parkinson em 11 anos foi finalmente aprovada globalmente. Felizmente, começaremos a ver a aprovação de mais opções terapêuticas para pacientes necessitados. Original em inglês, tradução Google, revisão Hugo. Fonte: Labiotech.
A Synpromics, com sede em Edimburgo, na Escócia, é uma empresa que se concentra no controle de genes. A biotecnológica decidiu colocar sua tecnologia para o desenvolvimento de uma terapia genética para Parkinson em colaboração com o University College London (UCL), uma universidade com uma forte experiência no desenvolvimento de terapias genéticas.
Como parte da colaboração de dois anos, a Synpromics criará promotores de genes sintéticos para controlar a expressão de um gene terapêutico em subpopulações neuronais específicas no sistema nervoso central (SNC). Esta abordagem de abordar apenas alvos específicos tem o potencial de reduzir os efeitos colaterais e tornar a terapia mais segura e eficaz.
Synpromics cria promotores de genes sintéticos projetados para otimizar a expressão em alvos específicos usando seu banco de dados de bioinformática PromPT.
A UCL incorporará os interruptores de genes desenvolvidos pela Synpromics no desenvolvimento de uma terapia genética para doença de Parkinson de início jovem (YOPD) em pacientes que começam a mostrar os sintomas de Parkinson antes de 50.
A terapia de genes para Parkinson não é um conceito novo. No Reino Unido, a Oxford BioMedica já completou um estudo de Fase I / II, onde mostrou que esta tecnologia poderia melhorar a função motora. Nos Estados Unidos, a Voyager Therapeutics completou um teste de Fase I este ano com resultados positivos.
Em comparação, Synpromics e UCL ainda estão em estágio inicial, mas sua abordagem para tornar o tratamento altamente específico pode trazer uma diferença em termos de segurança e eficácia. Especialmente em uma doença em que novos tratamentos são necessários desesperadamente. Este ano, a primeira droga nova para Parkinson em 11 anos foi finalmente aprovada globalmente. Felizmente, começaremos a ver a aprovação de mais opções terapêuticas para pacientes necessitados. Original em inglês, tradução Google, revisão Hugo. Fonte: Labiotech.
quarta-feira, 1 de novembro de 2017
Sanofi sai da sociedade com a Voyager de terapia genética de Parkinson na fase 2/3
A Voyager definiu a decisão como resultado do desejo da Sanofi de possuir os direitos nos EUA à terapia genética.
Oct 31, 2017 - Sanofi afastou-se da terapia genética de Parkinson coberta por sua aliança de US $ 845 milhões com a Voyager Therapeutics. A decisão dá à Voyager os direitos globais completos para o VY-AADC, mas deixa-a sem um parceiro à medida que se prepara para um processo clínico global de fase 2/3 global.
A Voyager enquadrou a decisão de Sanofi como resultado do desejo da Big Pharma de possuir os direitos nos EUA à terapia genética. O acordo de 2015 deu a Sanofi uma opção para retirar os ex-direitos nos EUA sobre a terapia do Parkinson. Na época, a Sanofi estava feliz o suficiente para montar US $ 100 milhões e se comprometer com US $ 745 milhões em marcos para essa opção e direitos sobre outros programas. Mas, na narração da história da Voyager, a atitude de Sanofi mudou nos últimos dois anos.
Essa mudança levou a discussões sobre a partilha de direitos dos Estados Unidos, mas a Voyager não estava disposta a afrouxar seu alcance no território.
"Nós não estávamos interessados em compartilhar os direitos nos EUA do programa", disse o CEO da Voyager, Steven Paul, em uma teleconferência com investidores para discutir as notícias. "Vemos um enorme valor ... na retenção de direitos sobre nosso programa de doença de Parkinson nos EUA"
Se, como diz Voyager, a decisão de Sanofi foi motivada pelos direitos nos EUA, ao invés de duvidas sobre o programa, levanta a questão do que mudou desde que atingiu o acordo original. Uma possibilidade é que o fracasso da Glybera da UniQure e o início lento do Strimvelis da GlaxoSmithKline na Europa colocaram a Sanofi fora da perspectiva de comercializar a terapia genética de Parkinson na região.
Glybera e Strimvelis sempre foram destinados a serem produtos de nicho. A Voyager está lançando seu candidato em um mercado muito maior, ou seja, os 10 000 pacientes de Parkinson estimados por ano que sofrem estimulação cerebral profunda (DBS). A Europa desempenhou um papel central na ascensão do DBS e continua a ser um importante mercado. O Japão, com o envelhecimento da população, é outro lugar onde o VY-AADC pode ter sucesso.
Paul falou sobre as perspectivas da VY-AADC nos territórios norte-americanos para investidores, mas a Europa reconhecida coloca desafios específicos.
"Há consideravelmente mais pressões de preços na Europa do que nos EUA", afirmou Paul.
A tarefa de navegar nessas pressões de preços pode, em última instância, cair em um novo parceiro ainda não identificado. A Voyager está confiante de que pode vender a própria terapia genética nos EUA e usá-la como uma plataforma de lançamento para sua evolução em uma organização de estágio comercial. Mas Paul parece aberto a descarregar direitos regionais se ocorrer um acordo que permita à Voyager manter o controle que priorizou.
"É fundamental que lideremos e gerenciemos o desenvolvimento clínico nós mesmos", afirmou Paul.
Nessa frente, a Voyager está trabalhando para manter o programa de desenvolvimento em progresso. Embora aceitar o envolvimento da Sanofi poderia ter ajudado nos EUA. Parte do teste de fase 2/3, Paul disse que a Voyager está em boa forma indo para o estudo.
Os pequenos volumes de fármacos de estudo necessários para a administração direta do cérebro da terapia genética permitiram à Voyager manter o controle da fabricação mesmo antes da separação da Sanofi. E Paul não vê outros aspectos da saída de Sanofi que impeçam a Voyager de começar a administrar a fase 2/3 no primeiro semestre do próximo ano.
As ações da Voyager caíram até 19% na sequência da notícia, antes de se estabilizarem 10% à medida que os esforços de mitigação de danos da biotecnologia começaram. Original em inglês, tradução Google, revisão Hugo. Fonte: Fierce Biotech. Veja mais aqui: Wired News Voyager Therapeutics Declared Longer-term Data from Phase-1b Trial Of VY-AADC for Advanced Parkinsons Disease.
segunda-feira, 11 de setembro de 2017
Fase 1b Trial de VY-AADC01 terapia genética para doença de Parkinson avançada mostra resultados positivos
SEPTEMBER 8, 2017 - Uma fase contínua da fase 1b de VY-AADC01, uma terapia genética para o tratamento da doença de Parkinson avançada (PD), está mostrando resultados positivos, incluindo melhora da função motora e atividades da vida diária, efeitos clínicos duráveis e boa tolerabilidade.
O anúncio foi feito pela Voyager Therapeutics, a empresa de terapia genética especializada em doenças neurológicas que lidera o julgamento.
Em dados anteriormente apresentados na Reunião Anual de 2017 da Academia Americana de Neurologia (AAN) e no Encontro Científico Anual da Associação Americana de Cirurgiões Neurológicos (AANS), a Voyager descreveu as motivações por trás do desenvolvimento da terapia gênica, bem como os resultados iniciais.
O VY-AADC01 foi desenvolvido para fornecer e promover diretamente a expressão da enzima L-aminoácido descarboxilase aromática (AADC), que é responsável pela transformação da levodopa em dopamina. O VY-AADC01 funciona promovendo a expressão do AADC em uma região cerebral específica chamada putamen.
A terapia baseia-se no pressuposto de que, como os pacientes com DP avançada não apresentam degeneração dos neurônios responsivos à dopamina nesta região do cérebro, a promoção de neurônios putamen para transformar levodopa em dopamina poderia potencialmente reduzir os sintomas motores da DP após uma única administração.
Seguindo os resultados positivos de um ensaio clínico de Fase 1a (NCT01973543) apresentado na AAN e AANS, os resultados do novo ensaio da Fase 1b (NCT03065192) são igualmente promissores.
No geral, os resultados demonstraram uma melhoria durável, dependente da dose e dependente do tempo em várias medidas da função motora após uma única administração de VY-AADC01. As medidas incluíram relatórios de pacientes, escalas de classificação de PD e atividades da vida diária.
O estudo da Fase 1b incluiu 15 pacientes com DP avançada e incapacitantes das flutuações motoras que foram tratados com uma dose única de VY-AADC01.
O objetivo principal é avaliar a segurança e distribuição da terapia genética administrada sob orientação de ressonância magnética (MRI) para a região do cérebro de putamen.
Os objetivos secundários incluem medidas da expressão e da atividade da AADC no putamen, medido por exames de tomografia por emissão de pósitrons (PET) e avaliações da função motora e atividades diárias, conforme medido pela Escala de Avaliação da Doença de Parkinson Unificada (uma medida da gravidade da DP) qualidade de vida e um diário completado pelo paciente.
Os pacientes foram divididos em três grupos de cinco, com cada grupo recebendo doses ascendentes de VY-AADC01. Os dados foram coletados aos 24 meses para o grupo um, 12 meses para o grupo dois e seis meses para o grupo três.
A seguir estão algumas das observações:
VY-AADC01 melhorou as medidas múltiplas da função motora dos pacientes e as atividades da vida diária nos grupos dois e três.
O VY-AADC01 aumentou a atividade enzimática de AADC de putaminal médio em 13% no grupo um, 56% no grupo dois e 79% no grupo três aos seis meses em relação à linha de base. A cobertura da actividade da enzima putamen e AADC mostrou-se altamente correlacionada.
O VY-AADC01 resultou em doses diárias reduzidas de levodopa oral (e medicamentos relacionados) para alcançar o controle motor ideal, sugerindo que os pacientes poderiam fazer mais dopamina com doses mais baixas de levodopa oral.
Os medicamentos para Parkinson foram reduzidos em média 208 mg (14%), 553 mg (34%) e 618 mg (42%) para os grupos um, dois e três, respectivamente, aos seis meses, em comparação com a linha de base.
Além disso, o VY-AADC01 foi encontrado para aumentar o "tempo de espera" dos pacientes sem discinesia (comprometimento do movimento voluntário) de 10,5 horas para 13,5 horas e para reduzir o "tempo de folga", como auto-relatado em seus diários.
Todos os 15 pacientes tiveram infusões VY-AADC01 bem-sucedidas que foram bem toleradas, sem eventos adversos sérios relacionados ao vetor (SAEs).
Quatorze dos 15 pacientes foram dispensados do hospital dentro de dois dias após a cirurgia.
Conforme relatado anteriormente, um paciente experimentou dois eventos adversos: uma embolia pulmonar, ou coágulo de sangue nos pulmões, e arritmia cardíaca relacionada, ou batimentos cardíacos irregulares.
Conseqüentemente, a profilaxia da trombose venosa profunda foi adicionada ao protocolo e não foram observados eventos subsequentes.
"Estamos muito satisfeitos com os resultados atualizados do nosso teste de aumento de dose. Em seis meses na Coorte 3, os pacientes obtiveram melhorias clinicamente significativas nos sintomas motores que foram observados na Coorte 2 e com doses ainda mais baixas de seus medicamentos orais de Parkinson, incluindo levodopa ", disse Bernard Ravina, MD, MS, médico-chefe da Voyager. em um comunicado de imprensa. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
segunda-feira, 12 de dezembro de 2016
Terapia genética na doença de Parkinson
DECEMBER 11, 2016 -
Nova semana emocionante de uma pequena empresa de biotecnologia
chamada Voyager Therapeutics que está usando terapia gênica para
tratar doenças neurodegenerativas. Seu principal produto (VY-AADC01)
é focado na doença de Parkinson e os resultados iniciais parecem
muito positivos.
O comunicado de
imprensa indica que o tratamento é bem tolerado e tem efeitos
benéficos nas funções motoras do sujeito. Esta última parte é
muito interessante como o julgamento está sendo realizado em pessoas
com doença de Parkinson avançada.
 |
| Terapia genética para a doença de Parkinson. Fonte: Wiki.Epfl |
quarta-feira, 27 de julho de 2016
Novo estudo demonstra a segurança a longo prazo de terapia genética na doença de Parkinson
July 27, 2016 - Novos dados de segurança de um estudo de pacientes com doença de Parkinson avançada, cinco anos após a entrega mediada por transferência de genes do fator neuroprotetor neurturina diretamente para os cérebros dos pacientes não revelaram efeitos adversos graves relacionados com o tratamento. O perfil de segurança encorajador a longo prazo do vírus adeno-associado administrado cirurgicamente (AAV2) -a terapia genética neurturin é descrita num artigo em Human Gene Therapy.
No artigo "segurança a longo prazo dos pacientes com doença de Parkinson que recebem o AAV2-neurturina Transferência Gene (CERE-120)" William Marks, Jr., da Universidade da Califórnia, San Francisco, Tiffany Baumann, Isis Pharmaceuticals (Carlsbad, CA), e Raymand Bartus,
RTBioconsultants (San Diego, CA), representando o CERE-120 Grupo de estudo, descreve o desenho do estudo, que estendemos como de duração do acompanhamento dos 53 pacientes avaliados em comparação com estudos anteriores com a finalidade de identificar quaisquer problemas de segurança que pudesse apresentar meses ou anos após o tratamento.
"A longevidade de expressão do vetor AAV torna particularmente útil para o tratamento de doenças neurodegenerativas crônicas", diz Editor-in-Chief Terence R. Flotte, MD, Celia e Isaac Haidak Professor de Educação Médica e Dean, Provost, e Executive Vice-Chanceler, University of Massachusetts Medical School, Worcester, MA. "Estes dados de longo prazo corroboram a evidência de que o AAV irá revelar-se uma importante plataforma para o tratamento desta doença altamente debilitante." Original em inglês, tradução Google, revisão Hugo. Fonte: Novo estudo demonstra a segurança a longo prazo de terapia genética na doença de Parkinson. Original em inglês, tradução Google, revisão Hugo. Fonte: MedicalXpress.
No artigo "segurança a longo prazo dos pacientes com doença de Parkinson que recebem o AAV2-neurturina Transferência Gene (CERE-120)" William Marks, Jr., da Universidade da Califórnia, San Francisco, Tiffany Baumann, Isis Pharmaceuticals (Carlsbad, CA), e Raymand Bartus,
RTBioconsultants (San Diego, CA), representando o CERE-120 Grupo de estudo, descreve o desenho do estudo, que estendemos como de duração do acompanhamento dos 53 pacientes avaliados em comparação com estudos anteriores com a finalidade de identificar quaisquer problemas de segurança que pudesse apresentar meses ou anos após o tratamento.
"A longevidade de expressão do vetor AAV torna particularmente útil para o tratamento de doenças neurodegenerativas crônicas", diz Editor-in-Chief Terence R. Flotte, MD, Celia e Isaac Haidak Professor de Educação Médica e Dean, Provost, e Executive Vice-Chanceler, University of Massachusetts Medical School, Worcester, MA. "Estes dados de longo prazo corroboram a evidência de que o AAV irá revelar-se uma importante plataforma para o tratamento desta doença altamente debilitante." Original em inglês, tradução Google, revisão Hugo. Fonte: Novo estudo demonstra a segurança a longo prazo de terapia genética na doença de Parkinson. Original em inglês, tradução Google, revisão Hugo. Fonte: MedicalXpress.
Assinar:
Postagens (Atom)