July 17, 2018 - Uma das abordagens mais promissoras para parar o mal de Parkinson é atacar a proteína nociva alfa-sinucleína. Seis ensaios clínicos estão testando terapias com esse objetivo.
No Parkinson, a alfa-sinucleína aglomera-se para formar agregados chamados corpos de Lewy, que os cientistas acreditam serem tóxicos e levam a sintomas e progressão da doença. Se os pesquisadores puderem impedir que a proteína se agrupe em corpos de Lewy, eliminá-los ou impedir sua disseminação de célula para célula, eles podem parar a doença de Parkinson (DP).
A Fundação Michael J. Fox ajudou a promover o desenvolvimento de terapias com esse objetivo, financiando diretamente alguns dos seis projetos agora em testes em humanos e fornecendo recursos para ajudar a projetar outros. Aqui compartilhamos as atualizações mais recentes do campo de ensaios clínicos de alfa-sinucleína.
Introduzindo Anticorpos contra a Alfa-Sinucleína
Uma forma pela qual os cientistas estão indo atrás da alfa-sinucleína é com os anticorpos: os combatentes do sistema imunológico do corpo. A empresa de biotecnologia Prothena está em parceria com a Roche para testar o seu anticorpo (PRX002 / RO7046015) contra a alfa-sinucleína em pessoas recentemente diagnosticadas com DP. No mês passado, cientistas publicaram que o anticorpo das empresas era seguro em um ensaio de Fase I em pessoas com DP e reduziu os níveis de alfa-sinucleína em amostras de sangue. O ensaio da Fase II (chamado PASADENA) está sendo realizado na Áustria, França, Alemanha, Espanha e Estados Unidos. Saiba mais no site do estudo e veja uma lista de sites de recrutamento no site de avaliação do Fox MJFF.
A Biogen também está testando um anticorpo anti-alfa-sinucleína em pessoas com Parkinson em um estudo de Fase II (chamado estudo SPARK). A inscrição está em espera por um curto período enquanto a empresa analisa os dados da primeira parte do teste. Este hiato foi pré-planejado para avaliar a segurança e entender como diferentes doses funcionam no corpo. Fique atento ao nosso blog para saber quando o teste da Biogen está aceitando novos participantes e saiba mais sobre os critérios de elegibilidade no site do estudo. Você também pode se conectar ao seu site de estudos local no Fox Trial Finder.
A AstraZeneca e a Takeda estão juntas testando um anticorpo alfa-sinucleína em voluntários de controle em um único local em Dallas, Texas. Saiba mais e obtenha informações de contato para a equipe de avaliação.
Aproveitando o poder do sistema imunológico para proteger as células
A empresa austríaca AFFiRiS descobriu que a vacina, que leva o organismo a produzir anticorpos alfa-sinucleína (como a vacina contra a gripe), era segura e tolerável em uma série de estudos de Fase I financiados pela MJFF. Os estudos testaram seis doses ao longo de quatro anos e os cientistas observaram uma resposta imunitária. "Os escores clínicos para a DP permaneceram estáveis durante todo o período do estudo, no entanto, o estudo não foi desenvolvido e não tem o poder de avaliar a eficácia clínica", escreveu a empresa em um comunicado à imprensa. A AFFiRiS está planejando um ensaio de Fase II para investigar a eficácia da vacina.
Prevenção de agregados de proteína tóxica
A Neuropore, subsidiária da MJFF, formou uma parceria com a empresa farmacêutica UCB para desenvolver o composto NPT200-11 / UCB0599, que se liga à alfa-sinucleína e bloqueia sua acumulação. A UCB está planejando agora um estudo de Fase Ib para procurar segurança e tolerabilidade tanto em voluntários de controle quanto em pessoas com Parkinson em um único local de estudo na Europa.
Proclara (anteriormente Neurophage) está desenvolvendo NPT088, que pode se ligar a proteínas, incluindo alfa-sinucleína, beta-amilóide e tau. (Os dois últimos estão implicados na doença de Alzheimer e na demência frontotemporal.) O financiamento do MJFF ajudou a mostrar que o NPT088 reduz a agregação de proteínas em um modelo de DP. Proclara está realizando um estudo de Fase I em pessoas com Alzheimer porque existe uma ferramenta para visualizar a proteína beta-amilóide no cérebro, o que ajudará a avaliar o quão bem o NPT088 funciona. MJFF priorizou o desenvolvimento de um agente de imagem semelhante para a alfa-sinucleína. Se esse estudo for bem sucedido, o Proclara testará o NPT088 em pessoas com Parkinson. Saiba mais sobre o teste de Alzheimer.
Estas seis terapias estão avançando e ainda mais estão próximas e se preparando para testes em voluntários humanos.
Perguntas sobre participação em pesquisa clínica? Veja nosso Pacote de participantes de testes para vídeos e um guia para saber mais sobre o processo e o impacto da inscrição nos estudos. Original em inglês, tradução Google, revisão Hugo. Fonte: Michael J Fox, com vários links.
- Página inicial
- Preliminares
- Mensagem aos Recém Diagnosticados
- Matutando... e alguns textos
- Filmes Recomendados
- Cuidadores
- Habilitar legendas em vídeos Youtube
- DBS - Deep Brain Stimulation
- Celebridades com DP
- Parkinson- Recomeçando a vida (facebook) - artigos produzidos
- Roteiro para pesquisas no blog
- Mal de Parkinson (nosso antigo nome)
Mostrando postagens com marcador anti-sinucleína. Mostrar todas as postagens
Mostrando postagens com marcador anti-sinucleína. Mostrar todas as postagens
quarta-feira, 18 de julho de 2018
quarta-feira, 18 de abril de 2018
BIIB054 da Biogen mostra dados positivos na fase 1 do teste de Parkinson
APRIL 18, 2018 - O candidato ao tratamento de Parkinson BIIB054 foi bem tolerado e apresentou um perfil farmacológico favorável nos resultados clínicos preliminares da Fase 1.
A Biogen apresentará esses resultados na Reunião Anual da ANN da American Academy of Neurology em 2018, em Los Angeles, Califórnia, de 21 a 27 de abril. O Parkinson’s News Today estará cobrindo a conferência.
A apresentação “Estudo randomizado, duplo-cego, controlado por placebo, dose única ascendente do anticorpo anti-alfa-sinucleína BIIB054 em pacientes com doença de Parkinson” será feita às 15h30. PST 24 de abril.
Pessoas com doença de Parkinson geralmente exibem aglomerados compostos principalmente da forma agregada de uma proteína chamada alfa-sinucleína. Esses aglomerados resultam do dobramento incorreto da alfa-sinucleína em sua estrutura tridimensional e prejudicam severamente a comunicação das células nervosas. Os cientistas acreditam que os agregados de alfa-sinucleína se espalham de células doentes para saudáveis, ditando a progressão de Parkinson.
O BIIB054 é um anticorpo derivado de humanos que se liga à alfa-sinucleína agregada, impedindo a propagação da proteína aglomerada.
A Biogen conduziu um ensaio de Fase 1 controlado por placebo (NCT02459886) para avaliar a segurança, a tolerabilidade e a farmacocinética de uma série de doses únicas de BIIB054, em participantes saudáveis e pacientes com doença de Parkinson precoce. Farmacocinética refere-se à absorção, biodisponibilidade, distribuição, metabolismo e excreção do medicamento no organismo.
Os cientistas também analisaram a farmacocinética do BIIB054 no sangue dos participantes, juntamente com a imunogenicidade do composto experimental, ou a sua capacidade de induzir uma resposta imunitária no organismo.
Um total de 18 pacientes com Parkinson (47-75 anos, 13 homens) receberam aleatoriamente uma série de doses únicas de BIIB054 (15-45 mg / kg) ou placebo. Os indivíduos foram avaliados por 16 semanas com imagens clínicas cerebrais, eletrocardiograma (medição da atividade elétrica do coração) e avaliações laboratoriais.
A meia-vida do sangue da BIIB054 - o tempo necessário para uma redução de 50% na quantidade de um composto - foi de aproximadamente 30 dias nos pacientes com Parkinson. A quantidade média de BIIB054 no líquido cefalorraquidiano, que preenche o cérebro e a medula espinhal, foi de 0,4% em relação à do sangue.
Dados farmacocinéticos de voluntários saudáveis e pacientes com Parkinson foram semelhantes. Os complexos de BIIB054-sinucleína foram encontrados no sangue, confirmando a ligação da molécula à alfa-sinucleína.
A maioria dos eventos adversos foi leve e não relacionada ao tratamento com BIIB054.
"Os resultados preliminares do primeiro estudo da BIIB054 em pacientes com [Parkinson] mostram uma favorável [farmacocinética], segurança e perfis de tolerabilidade, fornecendo justificativa para um maior desenvolvimento clínico", escreveram os pesquisadores. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
A Biogen apresentará esses resultados na Reunião Anual da ANN da American Academy of Neurology em 2018, em Los Angeles, Califórnia, de 21 a 27 de abril. O Parkinson’s News Today estará cobrindo a conferência.
A apresentação “Estudo randomizado, duplo-cego, controlado por placebo, dose única ascendente do anticorpo anti-alfa-sinucleína BIIB054 em pacientes com doença de Parkinson” será feita às 15h30. PST 24 de abril.
Pessoas com doença de Parkinson geralmente exibem aglomerados compostos principalmente da forma agregada de uma proteína chamada alfa-sinucleína. Esses aglomerados resultam do dobramento incorreto da alfa-sinucleína em sua estrutura tridimensional e prejudicam severamente a comunicação das células nervosas. Os cientistas acreditam que os agregados de alfa-sinucleína se espalham de células doentes para saudáveis, ditando a progressão de Parkinson.
O BIIB054 é um anticorpo derivado de humanos que se liga à alfa-sinucleína agregada, impedindo a propagação da proteína aglomerada.
A Biogen conduziu um ensaio de Fase 1 controlado por placebo (NCT02459886) para avaliar a segurança, a tolerabilidade e a farmacocinética de uma série de doses únicas de BIIB054, em participantes saudáveis e pacientes com doença de Parkinson precoce. Farmacocinética refere-se à absorção, biodisponibilidade, distribuição, metabolismo e excreção do medicamento no organismo.
Os cientistas também analisaram a farmacocinética do BIIB054 no sangue dos participantes, juntamente com a imunogenicidade do composto experimental, ou a sua capacidade de induzir uma resposta imunitária no organismo.
Um total de 18 pacientes com Parkinson (47-75 anos, 13 homens) receberam aleatoriamente uma série de doses únicas de BIIB054 (15-45 mg / kg) ou placebo. Os indivíduos foram avaliados por 16 semanas com imagens clínicas cerebrais, eletrocardiograma (medição da atividade elétrica do coração) e avaliações laboratoriais.
A meia-vida do sangue da BIIB054 - o tempo necessário para uma redução de 50% na quantidade de um composto - foi de aproximadamente 30 dias nos pacientes com Parkinson. A quantidade média de BIIB054 no líquido cefalorraquidiano, que preenche o cérebro e a medula espinhal, foi de 0,4% em relação à do sangue.
Dados farmacocinéticos de voluntários saudáveis e pacientes com Parkinson foram semelhantes. Os complexos de BIIB054-sinucleína foram encontrados no sangue, confirmando a ligação da molécula à alfa-sinucleína.
A maioria dos eventos adversos foi leve e não relacionada ao tratamento com BIIB054.
"Os resultados preliminares do primeiro estudo da BIIB054 em pacientes com [Parkinson] mostram uma favorável [farmacocinética], segurança e perfis de tolerabilidade, fornecendo justificativa para um maior desenvolvimento clínico", escreveram os pesquisadores. Original em inglês, tradução Google, revisão Hugo. Fonte: Parkinsons News Today.
sábado, 25 de novembro de 2017
Virada de jogo na doença de Alzheimer?
SEPTEMBER 3, 2016 - Resultados emocionantes publicados nesta semana sobre um pequeno ensaio clínico de fase 1b de um novo tratamento para a doença de Alzheimer. Nesta publicação, devemos rever os achados do estudo e considerar o que eles podem significar para a doença de Parkinson. (…)
A doença de Alzheimer é a doença neurodegenerativa mais comum, representando 60% a 70% de todos os casos de demência. É uma condição neurodegenerativa progressiva, como a doença de Parkinson, que afeta cerca de 30 milhões de pessoas ao redor do mundo.
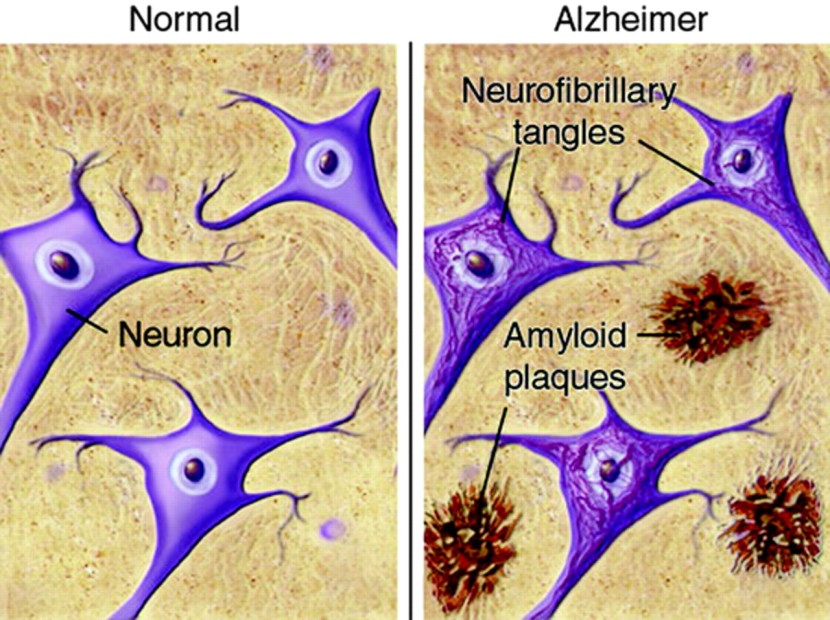
Dentro do cérebro, além da perda celular, a doença de Alzheimer é caracterizada pela crescente presença de duas características:
Emaranhados neurofibrilares
Placas amilóides
Os emaranhados são agregações de uma proteína chamada 'Tau' (voltaremos a Tau em uma postagem futura). Esses emaranhados residem nos neurônios inicialmente, mas à medida que a doença progride, os emaranhados podem ser encontrados no espaço entre células - que se acredita serem os últimos restos de uma célula moribunda.
As placas amilóides são conjuntos de proteínas que estão fora das células. Um componente chave da placa é beta amilóide. O beta-amilóide é um pedaço de uma proteína maior que fica na parede externa das células nervosas, onde possui certas funções. Em determinadas circunstâncias, enzimas específicas podem cortá-lo e flutuar.
Beta-amilóide é uma proteína muito "pegajosa" e acredita-se que as proteínas beta-amilóides flutuantes livres começam a aderir, aumentando gradualmente as grandes placas amilóides. E essas placas grandes foram consideradas envolvidas no processo neurodegenerativo da doença de Alzheimer. Assim, durante muito tempo os cientistas tentaram reduzir a quantidade de beta-amilóide livre no cérebro. Uma das principais maneiras de fazer isso é com anticorpos.
O que são anticorpos?
Um anticorpo é o fundamento do nosso sistema imunológico. É uma estrutura em forma de Y, que é usada para alertar o corpo quando um agente estranho ou insalubre está presente.
Dois braços fora do anticorpo em forma de Y têm o que é chamado de "locais de ligação de antigénios". Um antígeno é uma molécula que é capaz de induzir uma resposta do sistema imune (geralmente um agente estranho, mas pode ser uma célula doente / moribunda).
Atualmente, existem bilhões de anticorpos em seu corpo - cada um com conjuntos específicos de locais de ligação ao antígeno - aguardando a presença de seu antígeno. Os anticorpos estão presentes em duas formas: anticorpos secretos, livre flutuantes e anticorpos ligados à membrana. Os anticorpos secretos são produzidos por células B, que fazem parte do sistema imunológico. E é essa forma secreta de anticorpos que a ciência moderna usou para produzir novos medicamentos.
Mesmo? Como isso funciona?
Os cientistas podem produzir anticorpos no laboratório que visam proteínas específicas e, em seguida, injetar esses anticorpos no corpo de um paciente e enganar o sistema imunológico para remover essa proteína particular. Isso pode ser muito complicado, e é preciso ter certeza absoluta do design do anticorpo porque você não quer nenhum efeito "fora do alvo" - o sistema imunológico que remove uma proteína que se parece muito com a que você está direcionando.
Estes anticorpos fabricados são usados em muitas áreas diferentes de medicamentos, particularmente câncer (mais de 40 preparações de anticorpos foram aprovadas pela US Food and Drug Administration para uso em humanos contra câncer). Recentemente, grandes empresas farmacêuticas (como Biogen) tentaram usar esses anticorpos fabricados contra outras condições, como a doença de Alzheimer.
O que nos leva ao estudo publicado esta semana:
Abeta
Título: O anticorpo aducanumab reduz as placas de Aβ na doença de Alzheimer.
Neste estudo, o pesquisador realizou um estudo de 12 meses, duplo-cego, controlado por placebo do anticorpo Aducanumab. Este anticorpo se liga especificamente a agregados beta-amilóides potencialmente nocivos (pequenos e grandes). No início do teste, cada participante recebeu uma análise cerebral que permitiu que os pesquisadores determinassem o nível basal do beta-amilóide nos cérebros dos indivíduos.
Em conjunto, o estudo envolveu 165 pessoas, divididas aleatoriamente em cinco grupos diferentes: 4 grupos receberam as 4 concentrações diferentes do fármaco (1, 3, 6 ou 10 mg por kg) e 1 grupo que recebeu tratamento com placebo. Destes, 125 pessoas completaram o estudo, que tinha 12 meses de duração. A cada mês, eles receberam uma injeção do tratamento respectivo (lembre-se de que estes são anticorpos fabricados, o corpo não pode fazer este anticorpo específico, portanto deve ser repetido injetado).
Após 12 meses de tratamento, os indivíduos nos grupos 3, 6 e 10 mg por kg apresentaram uma redução significativa nos níveis de proteína beta-amilóide no cérebro (de acordo com imagens de varredura cerebral), indicando que o Aducanumab - o anticorpo injetado - estava fazendo o trabalho. Os indivíduos que receberam as maiores doses de Aducanumab apresentaram as maiores reduções no beta-amilóide no cérebro. Curiosamente, essa redução no beta-amilóide no cérebro foi acompanhada por uma desaceleração do declínio clínico conforme medido por testes de demência. Os indivíduos tratados com o placebo não viram qualquer redução nos níveis cerebrais de beta amilóide nem seu declínio clínico.
Os autores consideraram este estudo uma forte justificativa para ensaios maiores de fase III. Dois deles estão em andamento, com datas de conclusão esperadas em 2020.
Então, isso é uma coisa boa, certo?
Sim, este é um resultado muito emocionante para a comunidade de Alzheimer. Mas os resultados devem ser tomados com um grão de sal. Nós discutimos o beta-amilóide em uma publicação anterior (clique aqui para essa publicação (no original)). Embora tenha sido considerado o menino mau do mundo de Alzheimer, a função de beta-amilóide continua sendo objeto de debate. Alguns pesquisadores se preocupam com a remoção médica do cérebro, especialmente se tem funções positivas como propriedades anti-microbianas (ou combater doenças).
Dado que o tratamento é dado mensalmente e, portanto, pode ser controlado, podemos dormir facilmente sabendo que o desastre não ocorrerá nos pacientes que receberam o anticorpo. E se eles continuem a demonstrar uma desaceleração / parada da doença, isso representaria um passo MASSIVO no campo neurodegenerativo. Eu acho que o que estou dizendo é que é muito cedo para dizer. No entanto, será interessante ver o que acontece, pois esses pacientes são acompanhados ao longo do tempo. E os dois ensaios clínicos de fase 3 atualmente em curso, que envolvem centenas de participantes, fornecerão uma idéia mais definitiva de como o tratamento está funcionando. Então, o que isso tem a ver com a doença de Parkinson?
Sim, vamos voltar para a nossa área de interesse: a doença de Parkinson.
Biogen é a empresa farmacêutica que faz o anticorpo de Alzheimer (Aducanumab) discutido acima. Biogen também está atualmente realizando um teste de segurança de fase 1 (em adultos saudáveis normais) de um anticorpo que alveja a proteína associada à doença de Parkinson, alfa-sinucleína. Estamos aguardando ouvir os resultados desse ensaio. Várias outras empresas possuem abordagens baseadas em anticorpos para a doença de Parkinson (todas elas visando a proteína alfa-sinucleína).
Estas empresas incluem: Prothena - que completou os ensaios de segurança da fase 1 em março de 2015 (clique aqui para mais (no original))
Neuropore - que também completou os testes de segurança da fase 1 em março de 2015 (clique aqui para mais (no original))
Há algumas preocupações com essa abordagem, no entanto. Por exemplo, a alfa sinucleína é altamente expressa nos glóbulos vermelhos, e alguns pesquisadores se preocupam com o que afeta os anticorpos em sua função. Além disso, a alfa sinucleína tem sido suspeita de ter propriedades anti-virais - reduzindo a capacidade de vírus para infectar uma célula e replicar (clique aqui para ler mais sobre isso (no original)). Assim, a remoção de alfa-sinucleína pela injeção de anticorpos pode não ser necessariamente boa para o sistema de defesa do cérebro.
Ao contrário do beta-amilóide, no entanto, a maioria das atividades de alfa-sinucleína parecem ser realizadas dentro das paredes das células cerebrais, onde os anticorpos não podem tocá-lo. Assim, a esperança é que a única alfa sinucleína que está sendo afetada pelo tratamento de anticorpos seja a variedade que flua livremente ao redor do cérebro.
Os resultados do estudo de Alzheimer são um tremendo impulso para a abordagem de anticorpos para o tratamento de doenças neurodegenerativas e será muito interessante observar como isso funciona para a doença de Parkinson no futuro próximo. Original em inglês, tradução Google, revisão Hugo. Fonte: Science of Parkinsons.
A doença de Alzheimer é a doença neurodegenerativa mais comum, representando 60% a 70% de todos os casos de demência. É uma condição neurodegenerativa progressiva, como a doença de Parkinson, que afeta cerca de 30 milhões de pessoas ao redor do mundo.
Dentro do cérebro, além da perda celular, a doença de Alzheimer é caracterizada pela crescente presença de duas características:
Emaranhados neurofibrilares
Placas amilóides
Os emaranhados são agregações de uma proteína chamada 'Tau' (voltaremos a Tau em uma postagem futura). Esses emaranhados residem nos neurônios inicialmente, mas à medida que a doença progride, os emaranhados podem ser encontrados no espaço entre células - que se acredita serem os últimos restos de uma célula moribunda.
As placas amilóides são conjuntos de proteínas que estão fora das células. Um componente chave da placa é beta amilóide. O beta-amilóide é um pedaço de uma proteína maior que fica na parede externa das células nervosas, onde possui certas funções. Em determinadas circunstâncias, enzimas específicas podem cortá-lo e flutuar.
Beta-amilóide é uma proteína muito "pegajosa" e acredita-se que as proteínas beta-amilóides flutuantes livres começam a aderir, aumentando gradualmente as grandes placas amilóides. E essas placas grandes foram consideradas envolvidas no processo neurodegenerativo da doença de Alzheimer. Assim, durante muito tempo os cientistas tentaram reduzir a quantidade de beta-amilóide livre no cérebro. Uma das principais maneiras de fazer isso é com anticorpos.
O que são anticorpos?
Um anticorpo é o fundamento do nosso sistema imunológico. É uma estrutura em forma de Y, que é usada para alertar o corpo quando um agente estranho ou insalubre está presente.
Dois braços fora do anticorpo em forma de Y têm o que é chamado de "locais de ligação de antigénios". Um antígeno é uma molécula que é capaz de induzir uma resposta do sistema imune (geralmente um agente estranho, mas pode ser uma célula doente / moribunda).
Atualmente, existem bilhões de anticorpos em seu corpo - cada um com conjuntos específicos de locais de ligação ao antígeno - aguardando a presença de seu antígeno. Os anticorpos estão presentes em duas formas: anticorpos secretos, livre flutuantes e anticorpos ligados à membrana. Os anticorpos secretos são produzidos por células B, que fazem parte do sistema imunológico. E é essa forma secreta de anticorpos que a ciência moderna usou para produzir novos medicamentos.
Mesmo? Como isso funciona?
Os cientistas podem produzir anticorpos no laboratório que visam proteínas específicas e, em seguida, injetar esses anticorpos no corpo de um paciente e enganar o sistema imunológico para remover essa proteína particular. Isso pode ser muito complicado, e é preciso ter certeza absoluta do design do anticorpo porque você não quer nenhum efeito "fora do alvo" - o sistema imunológico que remove uma proteína que se parece muito com a que você está direcionando.
Estes anticorpos fabricados são usados em muitas áreas diferentes de medicamentos, particularmente câncer (mais de 40 preparações de anticorpos foram aprovadas pela US Food and Drug Administration para uso em humanos contra câncer). Recentemente, grandes empresas farmacêuticas (como Biogen) tentaram usar esses anticorpos fabricados contra outras condições, como a doença de Alzheimer.
O que nos leva ao estudo publicado esta semana:
Abeta
Título: O anticorpo aducanumab reduz as placas de Aβ na doença de Alzheimer.
Neste estudo, o pesquisador realizou um estudo de 12 meses, duplo-cego, controlado por placebo do anticorpo Aducanumab. Este anticorpo se liga especificamente a agregados beta-amilóides potencialmente nocivos (pequenos e grandes). No início do teste, cada participante recebeu uma análise cerebral que permitiu que os pesquisadores determinassem o nível basal do beta-amilóide nos cérebros dos indivíduos.
Em conjunto, o estudo envolveu 165 pessoas, divididas aleatoriamente em cinco grupos diferentes: 4 grupos receberam as 4 concentrações diferentes do fármaco (1, 3, 6 ou 10 mg por kg) e 1 grupo que recebeu tratamento com placebo. Destes, 125 pessoas completaram o estudo, que tinha 12 meses de duração. A cada mês, eles receberam uma injeção do tratamento respectivo (lembre-se de que estes são anticorpos fabricados, o corpo não pode fazer este anticorpo específico, portanto deve ser repetido injetado).
Após 12 meses de tratamento, os indivíduos nos grupos 3, 6 e 10 mg por kg apresentaram uma redução significativa nos níveis de proteína beta-amilóide no cérebro (de acordo com imagens de varredura cerebral), indicando que o Aducanumab - o anticorpo injetado - estava fazendo o trabalho. Os indivíduos que receberam as maiores doses de Aducanumab apresentaram as maiores reduções no beta-amilóide no cérebro. Curiosamente, essa redução no beta-amilóide no cérebro foi acompanhada por uma desaceleração do declínio clínico conforme medido por testes de demência. Os indivíduos tratados com o placebo não viram qualquer redução nos níveis cerebrais de beta amilóide nem seu declínio clínico.
Os autores consideraram este estudo uma forte justificativa para ensaios maiores de fase III. Dois deles estão em andamento, com datas de conclusão esperadas em 2020.
Então, isso é uma coisa boa, certo?
Sim, este é um resultado muito emocionante para a comunidade de Alzheimer. Mas os resultados devem ser tomados com um grão de sal. Nós discutimos o beta-amilóide em uma publicação anterior (clique aqui para essa publicação (no original)). Embora tenha sido considerado o menino mau do mundo de Alzheimer, a função de beta-amilóide continua sendo objeto de debate. Alguns pesquisadores se preocupam com a remoção médica do cérebro, especialmente se tem funções positivas como propriedades anti-microbianas (ou combater doenças).
Dado que o tratamento é dado mensalmente e, portanto, pode ser controlado, podemos dormir facilmente sabendo que o desastre não ocorrerá nos pacientes que receberam o anticorpo. E se eles continuem a demonstrar uma desaceleração / parada da doença, isso representaria um passo MASSIVO no campo neurodegenerativo. Eu acho que o que estou dizendo é que é muito cedo para dizer. No entanto, será interessante ver o que acontece, pois esses pacientes são acompanhados ao longo do tempo. E os dois ensaios clínicos de fase 3 atualmente em curso, que envolvem centenas de participantes, fornecerão uma idéia mais definitiva de como o tratamento está funcionando. Então, o que isso tem a ver com a doença de Parkinson?
Sim, vamos voltar para a nossa área de interesse: a doença de Parkinson.
Biogen é a empresa farmacêutica que faz o anticorpo de Alzheimer (Aducanumab) discutido acima. Biogen também está atualmente realizando um teste de segurança de fase 1 (em adultos saudáveis normais) de um anticorpo que alveja a proteína associada à doença de Parkinson, alfa-sinucleína. Estamos aguardando ouvir os resultados desse ensaio. Várias outras empresas possuem abordagens baseadas em anticorpos para a doença de Parkinson (todas elas visando a proteína alfa-sinucleína).
Estas empresas incluem: Prothena - que completou os ensaios de segurança da fase 1 em março de 2015 (clique aqui para mais (no original))
Neuropore - que também completou os testes de segurança da fase 1 em março de 2015 (clique aqui para mais (no original))
Há algumas preocupações com essa abordagem, no entanto. Por exemplo, a alfa sinucleína é altamente expressa nos glóbulos vermelhos, e alguns pesquisadores se preocupam com o que afeta os anticorpos em sua função. Além disso, a alfa sinucleína tem sido suspeita de ter propriedades anti-virais - reduzindo a capacidade de vírus para infectar uma célula e replicar (clique aqui para ler mais sobre isso (no original)). Assim, a remoção de alfa-sinucleína pela injeção de anticorpos pode não ser necessariamente boa para o sistema de defesa do cérebro.
Ao contrário do beta-amilóide, no entanto, a maioria das atividades de alfa-sinucleína parecem ser realizadas dentro das paredes das células cerebrais, onde os anticorpos não podem tocá-lo. Assim, a esperança é que a única alfa sinucleína que está sendo afetada pelo tratamento de anticorpos seja a variedade que flua livremente ao redor do cérebro.
Os resultados do estudo de Alzheimer são um tremendo impulso para a abordagem de anticorpos para o tratamento de doenças neurodegenerativas e será muito interessante observar como isso funciona para a doença de Parkinson no futuro próximo. Original em inglês, tradução Google, revisão Hugo. Fonte: Science of Parkinsons.
Assinar:
Postagens (Atom)